中国苏州,2026年3月25日——基石药业(股票代码:2616.HK),一家专注于肿瘤、免疫与炎症等关键疾病领域药物研发的创新驱动型生物医药企业,今日宣布公司核心商业化产品舒格利单抗再度获得欧洲肿瘤内科学会(ESMO)指南的【I, A】级推荐。此次,舒格利单抗被纳入《早期及局部晚期非小细胞肺癌动态临床指南》(Early and Locally Advanced Non-Small-Cell Lung Cancer Living Guideline),用于III期非小细胞肺癌(NSCLC)患者在同步或序贯放化疗后的巩固治疗。该推荐将显著助力舒格利单抗在欧盟及其他市场的准入进程,惠及更广泛的患者群体,从而为其全球商业化拓展提供坚实支持。
2025年2月,舒格利单抗联合化疗已获得ESMO《非驱动基因阳性转移性非小细胞肺癌动态临床指南》的【I, A】推荐,用于鳞状及非鳞状IV期非小细胞肺癌双适应症的一线治疗。至此,舒格利单抗在欧盟及英国获批的两项肺癌适应症均已被纳入ESMO指南,充分体现了其临床价值与国际肿瘤学界的认可。
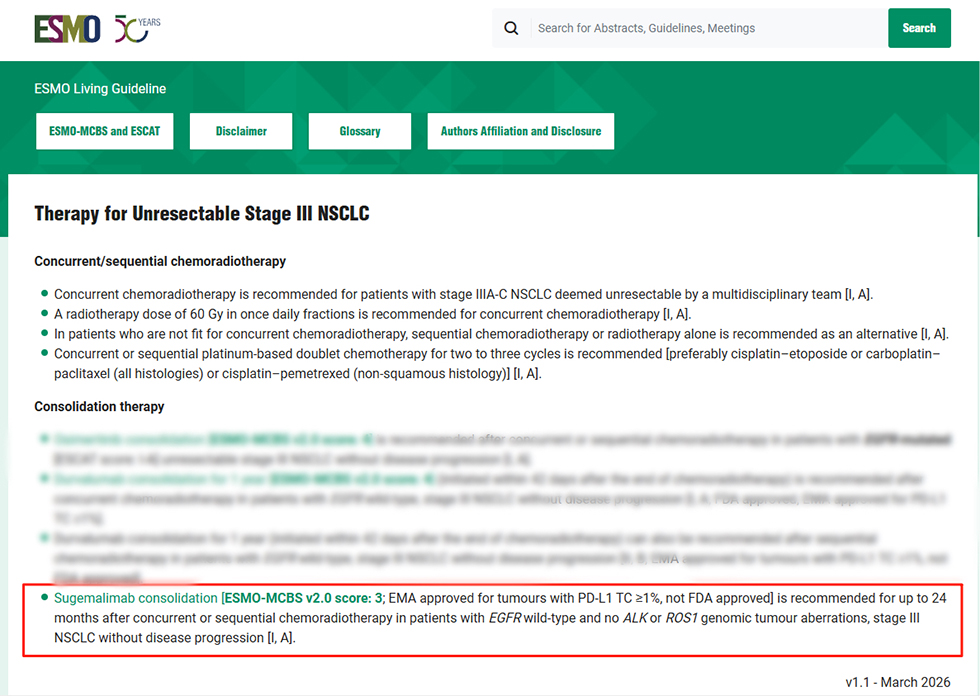
根据最新版ESMO指南明确推荐:
EGFR野生型、无ALK或ROS1基因突变的III期NSCLC患者,若在接受同步或序贯放化疗后未出现疾病进展,可采用舒格利单抗进行巩固治疗,治疗持续时间最长不超过24个月。该推荐适用于肿瘤细胞(TC)PD-L1表达水平≥1% 的患者【ESMO-临床获益量表(MCBS)v2.0评分:3分;已获欧洲药品管理局(EMA)批准】,证据等级为【I, A】。
指南中的治疗推荐是基于关键性III期临床试验GEMSTONE-301的研究结果,该研究证实,舒格利单抗用于III期NSCLC巩固治疗,能够为患者带来具有统计学意义的无进展生存期(PFS)改善和具有临床意义的总生存期(OS)延长。
截至目前,舒格利单抗已在欧洲、中东及非洲、拉丁美洲达成四项商业化合作,商业化网络已拓展至全球六十余个国家和地区,其市场准入申请也已在十余个国家获批或进入审评阶段,海外商业化布局正在稳步、高效推进中。
关于舒格利单抗注射液
舒格利单抗由基石药业基于OmniRat®转基因动物平台开发。该平台可一站式产生全人源抗体。作为一种全人源全长抗PD-L1单克隆抗体,舒格利单抗是一种最接近人体的天然G型免疫球蛋白4(IgG4)单抗药物,能降低在患者体内产生免疫原性及相关毒性的潜在风险。
欧盟委员会(EC)和英国药品和医疗保健用品管理局(MHRA)已批准舒格利单抗两项适应症:
目前,中国国家药品监督管理局(NMPA)已批准舒格利单抗五项适应症:
ESMO指南【I, A】推荐舒格利单抗:
关于基石药业
基石药业(香港联交所代码: 2616)成立于2015年底,是一家专注于肿瘤、免疫与炎症等关键疾病领域药物研发的创新驱动型生物医药企业,致力于满足中国和全球患者的殷切医疗需求。截至目前,公司已成功上市4款创新药、获批21项新药上市申请(NDA)以及9项适应症。当前研发管线均衡配置了抗体偶联药物(ADC)、多特异性抗体、以及免疫疗法和精准治疗药物在内的16款候选药物。同时,基石药业拥有一支资深管理团队,“全链条”覆盖临床前探索、临床转化、临床开发、药物生产、商务拓展、商业运营等关键环节。如需了解有关基石药业的更多信息,请访问:www.cstonepharma.com。
投资者关系: ir@cstonepharma.com
媒体关系:pr@cstonepharma.com
前瞻性声明
本文所作出的前瞻性陈述仅与本文作出该陈述当日的事件或资料有关。除法律规定外,于作出前瞻性陈述当日之后,无论是否出现新资料、未来事件或其他情况,我们并无责任更新或公开修改任何前瞻性陈述及预料之外的事件。请细阅本文,并理解我们的实际未来业绩或表现可能与预期有重大差异。本文内所有陈述乃本文章刊发日期作出,可能因未来发展而出现变动。
声明:仅供医疗卫生专业人士交流使用。