关键亮点:
中国苏州,2026年3月26日——基石药业(股票代码:2616.HK),一家专注于肿瘤、免疫与炎症等关键疾病领域药物研发的创新驱动型生物医药企业,今日公布其自主研发的PD-1/VEGF/CTLA-4三特异性抗体CS2009的最新临床进展。
基石药业首席执行官、研发总裁及执行董事杨建新博士表示:“基于CS2009目前取得的最新临床数据,我们对其在广泛瘤种中展现出的改变治疗格局的潜力充满信心。CS2009凭借独特的分子设计,在机制上形成了关键差异化优势。目前已有约200例患者入组,整体安全性表现突出,未观察到CTLA-4与PD-(L)1联合治疗中常见的严重毒性。
在疗效方面,CS2009在多个瘤种中均展现出亮眼结果:一线NSCLC单药治疗中,PD-L1 TPS≥50%人群的ORR达到90%;在免疫经治的后线非小细胞肺癌、非透明细胞肾细胞癌、软组织肉瘤等“冷肿瘤”中同样显示出显著优势。此外,在II期研究中,CS2009联合标准化疗用于一线NSCLC、CRC等多个适应症也取得了较高的客观缓解率。
我们期待在今年ASCO和(或)ESMO大会上公布更多I期和II期数据。目前我们正与多家全球跨国公司深入洽谈合作,并计划于2026年底前启动多项III期MRCT研究。”
患者入组迅速,I/II期数据印证优异安全性与有效性
CS2009的全球多中心I/II期临床试验正在澳大利亚和中国迅速累积临床数据,其II期新药临床试验(IND)申请也已获美国食品药品监督管理局(FDA)批准。截至2026年3月中旬,I期研究已共入组113例晚期实体瘤患者,中位随访期约为6个月;II期研究已共入组85例患者。
1、I期数据进一步验证CS2009优异的安全性:
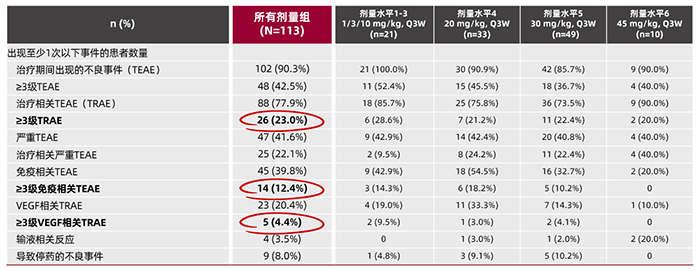
2、在IO经治肺癌与“冷肿瘤”中,凸显广谱抗肿瘤活性:
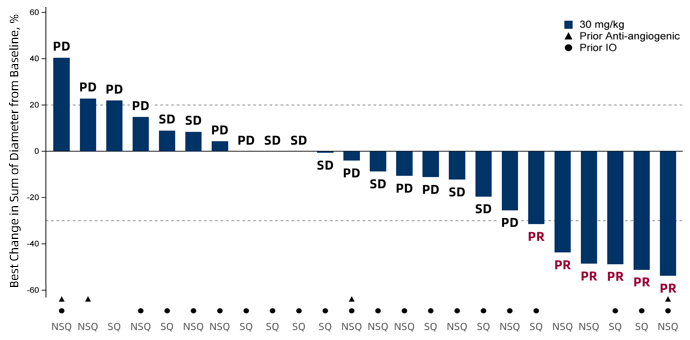
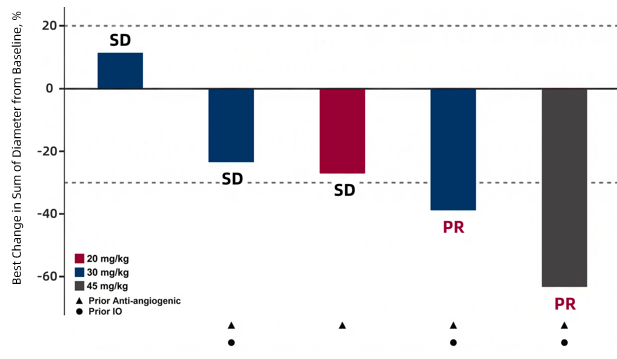
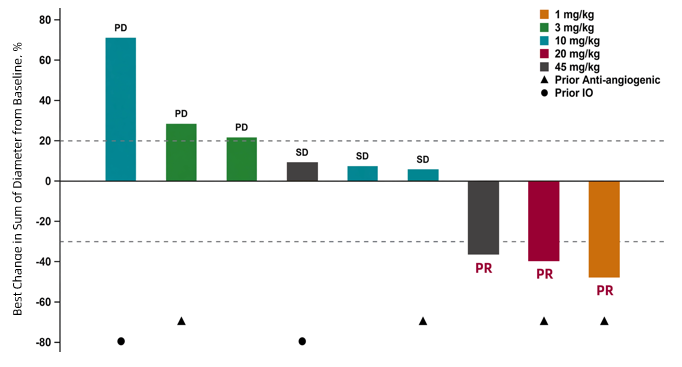
在所有剂量组中均观察到了CS2009的抗肿瘤活性,并在多个瘤种中显示出强效的抗肿瘤活性。
II期数据显示CS2009单药在一线NSCLC中ORR达90%,联合疗法在一线NSCLC和一线CRC中耐受性优异,初现变革性疗效潜力
CS2009全球多中心II期临床试验采用多队列平行扩展研究设计,旨在评估CS2009单药及联合疗法在9类实体瘤适应症(包括NSCLC、CRC、广泛期小细胞肺癌[ES-SCLC]、宫颈癌[CC]、胃癌或胃食管结合部癌[GC/GEJC]、食管鳞状细胞癌[ESCC]、铂类耐药卵巢癌[PROC]、三阴乳腺癌[TNBC]、肝细胞癌[HCC])的15个队列中的疗效和安全性。
1、一线NSCLC单药疗效亮眼:
CS2009单药(20 mg/30 mg, Q3W)在PD-L1 TPS≥50%的一线NSCLC患者(n=10)中,ORR达到 90%(9/10),DCR 为100%(10/10):
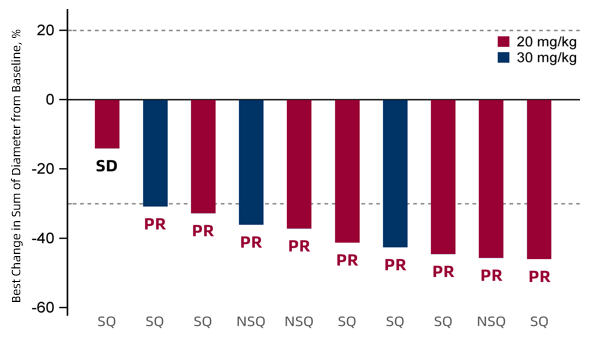
2、联合疗法展现优异耐受性和有前景的疗效:
多个CS2009联合标准化疗队列的安全性数据显示,CS2009联合疗法在多种肿瘤类型中,包括一线肺癌,一线结直肠癌等均表现出优异的耐受性,未增加化疗相关不良事件的发生率或严重程度,并已观察到初步强效抗肿瘤活性。
清晰高效的CS2009全球临床开发策略

基石药业计划于2026年底前启动CS2009首批III期MRCT,重点布局NSCLC、CRC、SCLC等适应症,加速这一创新疗法的全球开发进程。
更多CS2009的I期和II期临床研究数据预计将于2026年在ASCO年会和/或ESMO年会上公布。
关于CS2009(PD-1/VEGF/CTLA-4三特异性抗体)
CS2009是基石药业从分子设计开始自主研发的一款新型三特异性抗体,具备同类首创(FIC)/同类最佳(BIC)潜力。其靶向经临床验证的三个靶点——PD-1、VEGFA和CTLA-4,通过协同作用实现多维度的抗肿瘤效应。具体而言,阻断PD-1可逆转T细胞耗竭,阻断CTLA-4可促进T细胞活化和增殖,而阻断VEGFA则可抑制肿瘤血管生成,从而改善肿瘤微环境(TME)。在TME中,PD-1和CTLA-4的双重阻断作用通过与VEGFA的交联显著增强。同时,CS2009可优先结合PD-1和CTLA-4双阳性的肿瘤浸润T细胞,并最大程度上弱化对外周T细胞中CTLA-4调节通路的干扰。
关于基石药业
基石药业(香港联交所代码: 2616)成立于2015年底,是一家专注于肿瘤、免疫与炎症等关键疾病领域药物研发的创新驱动型生物医药企业,致力于满足中国和全球患者的殷切医疗需求。截至目前,公司已成功上市4款创新药、获批21项新药上市申请(NDA)以及9项适应症。当前研发管线均衡配置了抗体偶联药物(ADC)、多特异性抗体、以及免疫疗法和精准治疗药物在内的16款候选药物。同时,基石药业拥有一支资深管理团队,“全链条”覆盖临床前探索、临床转化、临床开发、药物生产、商务拓展、商业运营等关键环节。如需了解有关基石药业的更多信息,请访问:www.cstonepharma.com。
投资者关系: ir@cstonepharma.com
媒体关系:pr@cstonepharma.com
前瞻性声明
本文所作出的前瞻性陈述仅与本文作出该陈述当日的事件或资料有关。除法律规定外,于作出前瞻性陈述当日之后,无论是否出现新资料、未来事件或其他情况,我们并无责任更新或公开修改任何前瞻性陈述及预料之外的事件。请细阅本文,并理解我们的实际未来业绩或表现可能与预期有重大差异。本文内所有陈述乃本文章刊发日期作出,可能因未来发展而出现变动。
声明:仅供医疗卫生专业人士交流使用。